《自然·化学》报道多取代苯衍生物的程序化合成方法
更新日期:2015-03-03苯环是有机化学中最重要的结构单元之一,其上有6个氢原子可以被取代形成很多种衍生物。根据Burnside计数定理,n个取代基的可能取代结果N为(2n+2n2+4n3+3n4+n6)/12。例如,假如有10个取代基,可能产生的取代苯就有86185种可能。尽管有众多种可能性,但是很多功能化六苯基苯(hexaarylbenzenes,HABs)都是对称结构的。这主要是因为缺乏一种通用的、能完全控制取代位置的不对称多取代合成方法。
在这种现状驱动下,最近日本名古屋大学的Kenichiro Itami(伊丹健一郎)、Junichiro Yamaguchi(山口潤一郎)团队设计研发出一种特殊的顺序合成方法来制备5-取代或6-取代的苯衍生物。他们巧妙地结合了C-H键活化、交叉偶联以及[4+2]环加成反应等合成手段,通过共有的起始化合物3-甲基噻吩,程序化地合成了六芳基苯化合物。上述研究成果发表于2015年3月份出版的《自然·化学》杂志上(Nat. Chem., 2015, 7, 227-233, DOI: 10.1038/nchem.2174),展示了首例用程序合成法在苯环的所有位置上代入不同的指定芳香基团。该方法不仅开辟了作为重要药物前体和化工材料的多取代苯的广阔合成空间,还可以用于其它复杂化合物(如四芳基萘和五芳基吡啶)的程序化合成。
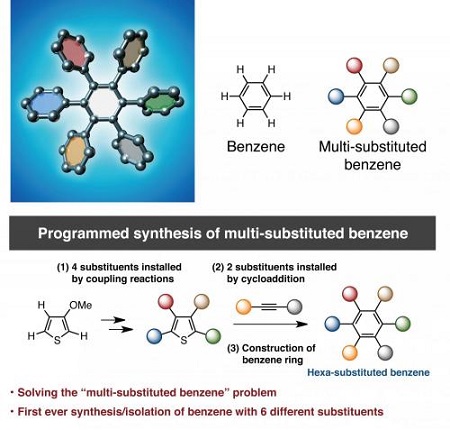
图:多取代苯的程序化合成,来源:名古屋大学
该团队利用他们组知名的镍催化剂,该催化剂可以被用于杂环上C-H的偶联。首先合成四芳基取代噻吩,然后再通过与芳基乙炔进行Diels-Alder反应最终得到六个不同芳基取代的苯环产物,这也是该类化合物的首次合成,具有里程碑的意义。
“合成HABs的关键步骤是用噻吩(一种含有硫原子的5元环)作为起始原料”,Yamaguchi说。“2009年我们曾通过C-H活化的方式程序合成了含有4个不同芳基的噻吩,现在我们改进了这一方法并将其延伸到多取代苯的合成上。”
“在取代的噻吩上,我们进行了一系列的金属-催化偶合反应,然后进行闭环反应形成HAB。”论文的共同作者Suzuki 和Segawa说。“经过若干次寻找合适的反应条件,我们最终合成了这种具有螺旋状辐射延伸晶体结构的、六个不同取代基的HAB”。
研究人员也对他们所合成化合物的荧光性质进行了一系列的实验测试,结果表明通过对外部基团的调节可以让原本无荧光属性的六苯基苯具有荧光特性。
具体合成细节:
中间体四芳基取代噻吩的合成法
论文作者首先以3-甲氧基噻吩作为原料,该原料有两大优势,第一,可以很容易地在2位选择性地导入取代基,另外环氧基在最后也能够很容易地转换成芳基。
最开始的芳基的导入本来可以用他们比较擅长的直接C-H偶联法得到,但是考虑到该起始原料需要大量合成制备,所以首先在噻吩的2位引入Br,然后使用铃木-宫浦偶联反应(Suzuki-Miyaura reaction)在2位选择性地导入了第一个芳基取代基。
接着终于到了C-H偶联反应该出场的时候了。在这里也是为了能够顺利的大量合成该化合物,作者改良了已知条件,顺利的在噻吩的4位导入了再一个芳基取代基。
剩下的5位同样也是利用C-H偶联引入第三个芳基后,通过3位剩下的甲氧基作为支架,利用铃木-宫浦反应导入了最后一个芳香基,最终完成了四芳基取代噻吩中间体的合成。
苯环骨架的构建
虽然看似简单的这步,仅仅只是利用Diels-Alder反应构筑苯环骨架,但是寻找合适的反应条件花费了大量的时间。首先氧化噻吩,在当量以上的三氟化硼的存在下,加入氧化剂mCPBA选择性的把噻吩氧化成S-氧化物,然后与芳基乙炔在高温条件下进行Diels-Alder反应脱去氧化硫形成苯环骨架,最终成功得到六不同芳基取代的苯环。
很遗憾的是Diels-Alder反应的方向选择性比较差,最终得到了位置异构的混合产物,但是作者还是很努力的尝试重结晶,貌似分离纯化得到了单一的产物。
虽然得到了纯物质,但是该化合物的结构鉴定还是一个难题。另外分离位置异构体还有另一种比较简便的方法,把一个芳基酮取代基的酮还原,再把还原后的羟基用TBS保护,作者发现得到的TBS保护的异构体用TLC就能很简便的分离,同时得到的纯物质很容易析出单晶,最终通过X-ray确定了化合物的立体构造。
通过X-ray解析结果,我们可以看到,该化合物上的芳香环取代基按照各自角度排列着,真心十分漂亮。
程序化合成
正如作者所述,该方法被他们称为程序化合成法。只要改变一下反应中使用的芳香基底物,我们就可以自由地改变引入噻吩中的芳基取代基。另外一个芳基乙炔原料也可以简单地制备,所以利用该方法可以自由地合成任意组合的六芳基取代苯环产物。
(杨琛 综合新材料在线、化学空间Chem-Station报道)
相关阅读:物理学家组织网报道(英文)