北大深研院实现非过渡金属催化的Suzuki反应
更新日期:2018-03-12有机硼试剂和有机亲电试剂的偶联反应,即Suzuki-Miyaura偶联反应是目前人们构建碳-碳键最行之有效的方法,2010年诺贝尔奖的颁发更加印证了其对人类社会的贡献。在过去的50年中,过渡金属作为催化剂在这类反应的发展中扮演了核心角色,但由于过渡金属催化本身的反应特性限制,也面临着诸多挑战。例如sp2杂化的芳基卤代烃反应活性高于sp3杂化的烷基卤代烃,当分子中存在多种碳-卤键时,选择性地优先转化烷基碳-卤键就是一大难题。
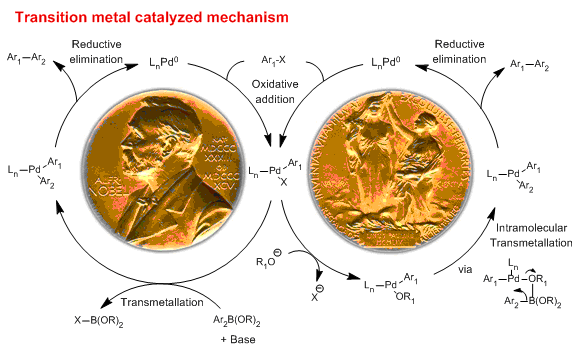
Suzuki反应
北京大学深圳研究生院黄湧课题组针对这样的问题,另辟蹊径,提出了寻找有别于过渡金属催化的偶联过程,实现非过渡金属催化或者无过渡金属催化机制下的Suzuki偶联反应的目标设想。他们认为,新催化机制的引入,可以提供与传统过渡金属催化过程相互补的反应活性,将会对目前现有的合成方法学做出极大的补充。针对该目标,黄湧课题组发展了新型有机硫醚类催化剂,实现了首例由非过渡金属而是有机小分子作为催化剂的Suzuki偶联反应,该成果近日发表于《美国化学会志》上,题为“A Transition-Metal-Free Suzuki-Type Cross-Coupling Reaction of Benzyl Halides and Boronic Acids via 1,2-Metallate Shift”(J. Am. Chem. Soc., 2018, DOI: 10.1021/jacs.8b00380)。
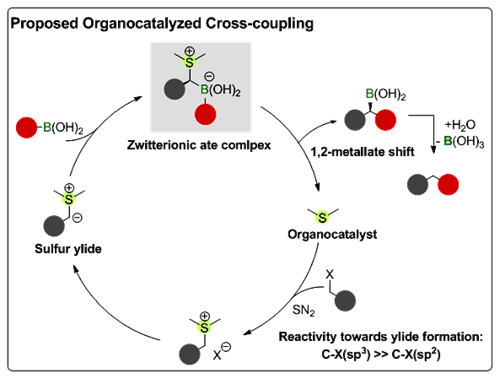
有机小分子催化的Suzuki偶联反应
该课题组受到有机硼化合物1,2-迁移反应(1979年诺贝尔奖反应)以及硫叶立德化学的启发,利用基础有机化学中亲核取代反应对于烷基亲电试剂和芳基亲电试剂的分辨能力,构想出一个同时含有正负电荷的中间体(zwitterionic ate complex),以此为基础,推演出有机小分子催化机理,并以苄基卤代烃和芳基苯硼酸作为模型反应进行研究,优化催化剂结构,最终不仅实现了首例非过渡金属催化的Suzuki反应,还获得了和传统过渡金属催化机制相互补的反应活性。新催化体系中,对烷基亲电试剂选择性要远高于芳基亲电试剂。传统偶联反应中最为活泼的芳基碳-碘键和芳基碳-溴键在新催化体系下并不不受影响,产物中可以得到保留,并且为后续流水式衍生化合成提供了反应位点。而初步的机理实验,也验证了设计的催化机制,为以后交叉偶联反应的发展提供了新思路。
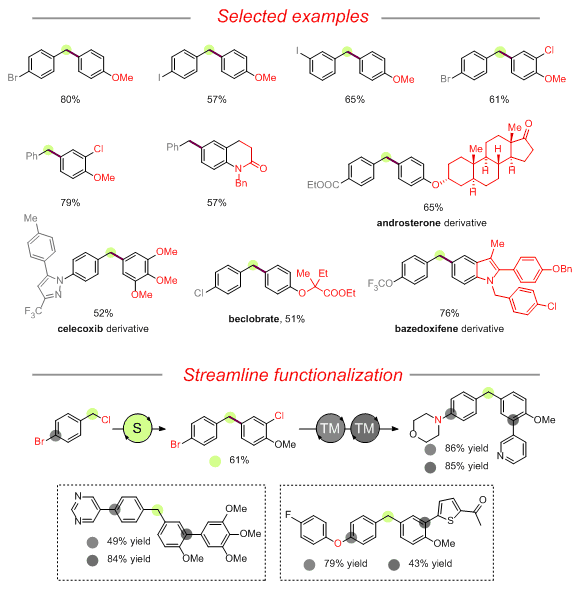
代表性底物及应用
(来源:北京大学新闻网)